02/11/2015
Mg++: Médicament de la coagulopathie ?
Both acute delivery of and storage with magnesium sulfate promote cold-stored platelet aggregation and coagulation function
Meledeo MA et Al. J Trauma Acute Care Surg. 2015 Oct;79(4 Suppl 2):S139-45
----------------------------------------
Il y a quelque mois était publié un travail de recherche portant sur l'intérêt de l'administration de Adénosine/Lidocaïne/Mg2+ ALM (1, 2, 3). Une hypothèse faite par les auteurs serait que L'ALM agirait comme un antifibrinolytique en activant la voie du thrombin-activatable fibrinolysis inhibitor (TAFI) plutôt que celle de la protéine C. Cette action passerait par un mécanisme antiinflammatoire, une modification de la polarité endothéliale et une action sur la fonction plaquettaire. Le travail expérimental dont l'abstract est présenté met en avant l'intérêt de l'adminsitration de magnésium pour la restauration de la fonction plaquettaire après conservation de palquettes d'aphérèse au delà de 5 jours.
----------------------------------------
BACKGROUND:
The platelet storage lesion causes loss of function and viability over time. A new paradigm for platelet storage is desired to enable safer, more effective transfusions while reducing waste. We hypothesized that repletion of Mg, which is chelated by citrate anticoagulant, could reduce platelet storage lesion severity when given in conjunction with storage at a refrigerated temperature.
METHODS:
Apheresis platelet units were collected from healthy donors and stored at 22°C or 4°C. On Days 0, 2, 4, and 8, samples were collected for analyses of receptor-mediated aggregation, coagulation, adhesion to collagen under flow, and viability. In the first series, samples were given anacute dose of MgSO4 before testing; in the second series, storage bags were supplemented with 0-, 3-, or 6-mM MgSO4.
RESULTS:
Acutely delivered MgSO4 induced a more rapid coagulation time in apheresis platelets, further enhanced by storage at 4°C. Plateletadhesion to a collagen surface while exposed to arterial shear rates (920 s) was enhanced by MgSO4 supplementation-acute MgSO4 had a large effect on adhesion of fresh platelets, which diminished more rapidly in 22°C samples, while storage with MgSO4 showed significant benefits even out to Day 4 at both temperatures. Although 4°C storage improves the longevity of platelet aggregation responses to agonists, MgSO4 supplementation did not change those responses.
CONCLUSION:
Acute MgSO4 reduces clot time likely through the transient increase of free Ca. Limited differences between platelet function inacute delivery of and storage with MgSO4 diminish the possibility that Mg-induced metabolic inhibition of platelets synergizes with 4°C storage. Regardless, magnesium supplementation to platelets is an exciting possibility in transfusion because the adhesion response of 22°C-stored platelets on Day 4 is significantly enhanced when stored with 6-mM MgSO4
| Tags : coagulopathie
23/10/2015
Quelle place pour les facteurs de la coagulation ?
| Tags : hémorragie, coagulopathie, choc
18/09/2015
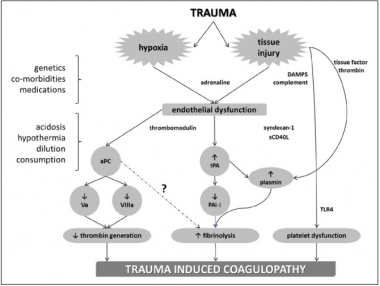
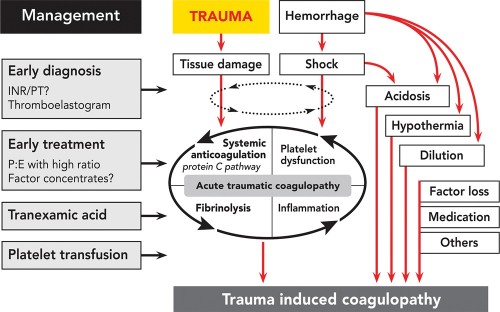
Coagulopathie traumatique: Mécanismes
Trauma-Induced Coagulopathy: An Institution's 35 Year Perspective on Practice and Research
Gonzales E. et Al. Scandinavian Journal of Surgery 103: 89–103, 2014
| Tags : coagulopathie
03/07/2015
Fibrinogène avec le TXA ?: Plutôt oui
Association of Cryoprecipitate and Tranexamic Acid With Improved Survival Following Wartime Injury: Findings From the MATTERs II Study
Morrison JJ et Al. JAMA Surg. 2013;148(3):218-225.
Objective To quantify the impact of fibrinogen-containing cryoprecipitate in addition to the antifibrinolytic tranexamic acid on survival in combat injured.
Design Retrospective observational study comparing the mortality of 4 groups: tranexamic acid only, cryoprecipitate only, tranexamic acid and cryoprecipitate, and neither tranexamic acid nor cryoprecipitate. To balance comparisons, propensity scores were developed and added as covariates to logistic regression models predicting mortality.
Setting A Role 3 Combat Surgical Hospital in southern Afghanistan.
Patients A total of 1332 patients were identified from prospectively collected UK and US trauma registries who required 1 U or more of packed red blood cells and composed the following groups: tranexamic acid (n = 148), cryoprecipitate (n = 168), tranexamic acid/cryoprecipitate (n = 258), and no tranexamic acid/cryoprecipitate (n = 758).
Main Outcome Measure In-hospital mortality.
Results Injury Severity Scores were highest in the cryoprecipitate (mean [SD], 28.3 [15.7]) and tranexamic acid/cryoprecipitate (mean [SD], 26 [14.9]) groups compared with the tranexamic acid (mean [SD], 23.0 [19.2]) and no tranexamic acid/cryoprecipitate (mean [SD], 21.2 [18.5]) (P < .001) groups. Despite greater Injury Severity Scores and packed red blood cell requirements, mortality was lowest in the tranexamic acid/cryoprecipitate (11.6%) and tranexamic acid (18.2%) groups compared with the cryoprecipitate (21.4%) and no tranexamic acid/cryoprecipitate (23.6%) groups. Tranexamic acid and cryoprecipitate were independently associated with a similarly reduced mortality (odds ratio, 0.61; 95% CI, 0.42-0.89; P = .01 and odds ratio, 0.61; 95% CI, 0.40-0.94; P = .02, respectively). The combined tranexamic acid and cryoprecipitate effect vs neither in a synergy model had an odds ratio of 0.34 (95% CI, 0.20-0.58; P < .001), reflecting nonsignificant interaction (P = .21).
Conclusions Cryoprecipitate may independently add to the survival benefit of tranexamic acid in the seriously injured requiring transfusion. Additional study is necessary to define the role of fibrinogen in resuscitation from hemorrhagic shock.
| Tags : coagulopathie
27/03/2015
Hypersalé: Mieux avec de la lidocaïne , du magnésium et de l'adénosine ?
Correction of acute traumatic coagulopathy with small-volume 7.5% NaCl adenosine, lidocaine, and Mg2+ occurs within 5 minutes: A ROTEM analysis
Hayley L. et Al. J Trauma Acute Care Surg. 2015;78: 773-783
------------------------------------------------------------------------------------------------
La prévention/correction de la coagulopathie traumatique est un axe essentiel de la réanimation du traumatisé grave. Le choix du soluté a son importance. L'adjonction de lidocaïne, de magnésium et d'adénosine au NaCl7,5% serait bénéfique. On observerait une fibrinolyse beaucoup moins importante qu'avec le salé hypertonique seul.
------------------------------------------------------------------------------------------------
BACKGROUND: Acute traumatic coagulopathy is a major contributor to mortality and morbidity following hemorrhagic shock. Our aim was to examine the effect of small-volume 7.5% NaCl with adenosine, lidocaine, and Mg2+ (ALM) resuscitation on the timing of correction of coagulopathy in the rat model of severe hemorrhagic shock using ROTEM.
METHODS: Male rats (300Y450 g, n = 64) were randomly assigned to (1) baseline, (2) sham, (3) bleed, (4) shock, (5) 7.5% NaCl for 5 minutes, (6) 7.5% NaCl with ALM for 5 minutes, (7) 7.5% NaCl for 60 minutes, or (8) 7.5% NaCl with ALM for 60 minutes (all n = 8). For resuscitation, 0.3-mL intravenous bolus of 7.5% NaCl was administered with and without ALM (n = 8 each group). Hemodynamics and coagulopathy were assessed.
RESULTS: After hemorrhage, prothrombin time (PT) and activated partial thromboplastin time (aPTT) increased approximately four to six times, and ROTEM indicated hypocoagulopathy. After 60-minute shock, no sustainable clots could form. 7.5% NaCl increased mean arterial pressure (MAP) to 46 T 2 mm Hg at 5 minutes and generated a weak clot in EXTEM with hyperfibrinolysis in all tests. At 60 minutes, 7.5% NaCl failed to sustain MAP (43 T 5 mm Hg) and generate a viable clot. In direct contrast, 7.5% NaCl with ALM at 5 minutes resuscitatedMAP to 64 T 3 mm Hg, corrected PT and aPTT, and generated fully formed EXTEM and FIBTEM clots. At 60 minutes, MAP was 69 T 5 mm Hg, PT and aPTT were fully corrected, and > angle, clot amplitudes (A10, A30), as well as clot firmness and elasticity were not significantly different from baseline. ALM clot lysis at 60 minutes was significantly less than bleed, shock, or 7.5% NaCl, indicating protection against hyperfibrinolysis.
CONCLUSION: Small-volume 7.5% NaCl failed to resuscitate and correct coagulopathy. In contrast, 7.5% NaCl with ALM resuscitated MAP and corrected coagulopathy at 5 minutes, with further improvements at 60 minutes in clot kinetics, propagation, and firmness. ALM fully reversed hyperfibrinolysis to baseline. The possible mechanisms are discussed. (J Trauma Acute Care Surg. 2015;78:
| Tags : remplissage, coagulopathie
04/09/2014
Remplissage vasculaire: Evolution majeure du TCCC
L'emploi préhospitalier de la transfusion de globules rouges et de plasma était évoqué de manière anecdotique. Une évolution importante survient dans la procédure américaine du TCCC (1, 2). Cette pratique est en passe de devenir une recommandation protocolée de théâtre pour les blessés en état de choc (Pas de pouls radial et conscience altérée el l'absence de traumatisme crânien) hémorragique avec notons le recours au Plyo du CTSA.
" Tactical Field Care and TACEVAC Care
7. Fluid resuscitation
a. The resuscitation fluids of choice for casualties in hemorrhagic shock, listed from most to least preferred, are: whole blood*; plasma, RBCs and platelets in 1:1:1 ratio*; plasma and RBCs in 1:1 ratio; plasma or RBCs alone; Hextend; and crystalloid (Lactated Ringers or Plasma-Lyte A).
b. Assess for hemorrhagic shock (altered mental status in the absence of brain injury and/or weak or absent radial pulse).
1. If not in shock:
- No IV fluids are immediately necessary.
- Fluids by mouth are permissible if the casualty is conscious and can swallow.
2. If in shock and blood products are available under an approved command or theater blood product administration protocol:
- Resuscitate with whole blood*, or, if not available
- Plasma, RBCs and platelets in a 1:1:1 ratio*, or, if not available
- Plasma and RBCs in 1:1 ratio, or, if not available;
- Reconstituted dried plasma, liquid plasma or thawed plasma alone or RBCs alone;
- Reassess the casualty after each unit. Continue resuscitation until a palpable radial pulse, improved mental status or systolic BP of 80-90 mmHg is present.
3. If in shock and blood products are not available under an approved command or theater blood product administration protocol due to tactical or logistical constraints:
- Resuscitate with Hextend, or if not available;
- Lactated Ringers or Plasma-Lyte A;
- Reassess the casualty after each 500 mL IV bolus;
- Continue resuscitation until a palpable radial pulse, improved mental status, or systolic BP of 80-90 mmHg is present.
- Discontinue fluid administration when one or more of the
above end points has been achieved.
4. If a casualty with an altered mental status due to suspected TBI has a weak or absent peripheral pulse, resuscitate as necessary to restore and maintain a normal radial pulse. If BP monitoring is available, maintain a target systolic BP of at least 90 mmHg.
5. Reassess the casualty frequently to check for recurrence of shock. If shock recurs, recheck all external hemorrhage control measures to ensure that they are still effective and repeat the fluid resuscitation as outlined above.
* Neither whole blood nor apheresis platelets as these products are currently collected in theater are FDA-compliant. Consequently, whole blood and 1:1:1 resuscitation using apheresis platelets should be used only if all of the FDA-compliant blood products needed to support 1:1:1 resuscitation are not avalaible
| Tags : choc, coagulopathie, remplissage
21/11/2013
Le plasma lyophilisé: Bon pour le cerveau du traumatisé qui saigne
Early treatment with lyophilized plasma protects the brain in a large animal model of combined traumatic brain injury and hemorrhagic shock
Imam AM et Al. J Trauma Acute Care Surg. 2013;75: 976-983
accéder aux abstracts de la WTA publiés dans J trauma Acute care
_____________________________________
Bien sûr une étude animale, mais une de plus qui milite pour un emploi précoce du plasma lyophylisé.
_____________________________________
BACKGROUND: Combination of traumatic brain injury (TBI) and hemorrhagic shock (HS) can result in significant morbidity and mortality. We have previously shown that early administration of fresh frozen plasma (FFP) in a large animal model of TBI and HS reduces the size of the brain lesion as well as the associated edema. However, FFP is a perishable product that is not well suited for use in the austere prehospital settings. In this study, we tested whether a shelf-stable, low-volume, lyophilized plasma (LSP) product was as effective as FFP.
METHODS:
Yorkshire swine (42-50 kg) were instrumented to measure hemodynamic parameters, intracranial pressure, and brain tissue oxygenation. A prototype, computerized, cortical impact device was used to create TBI through a 20-mm craniotomy: 15-mm cylindrical tipimpactor at 4 m/s velocity, 100-millisecond dwell time, and 12-mm penetration depth. Volume-controlled hemorrhage was induced(40-45% total blood volume) concurrent with the TBI. After 2 hours of shock, animals were treated with (1) normal saline (NS, n = 5), (2) FFP (n = 5), and (3) LSP (n = 5). The volume of FFP and LSP matched the shed blood volume, whereas NS was 3 times the volume. Six hours after resuscitation, brains were sectioned and stained with TTC (2, 3, 5-Triphenyltetrazolium chloride), and lesion size (mm3) and swelling (percent change in volume compared with the contralateral, uninjured side) were measured.
RESULTS:
This protocol resulted in a highly reproducible brain injury, with clinically relevant changes in blood pressure, cardiac output, tissue hypoperfusion, intracranial pressure, and brain tissue oxygenation. Compared with NS, treatment with LSP significantly ( p G 0.05) decreased brain lesion size and swelling (51% and 54%, respectively).
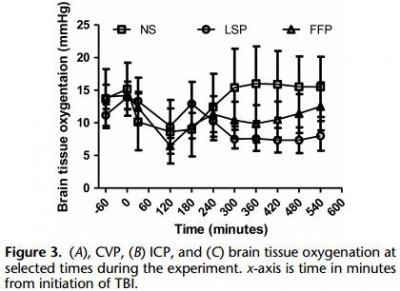
CONCLUSION: In a clinically realistic combined TBI + HS model, early administration of plasma products decreases brain lesion size and edema. LSP is as effective as FFP, while offering many logistic advantages.
| Tags : tbi, coagulopathie
07/08/2013
Plasma: En préhospitalier AUSSI +++
Point-of-injury use of reconstituted freeze dried plasma as a resuscitative fluid: A special report for prehospital trauma care
Glassberg E. et All. J J Trauma Acute Care Surg. 2013;75(Suppl 2):S111YS111.
La prise en charge d'hémorrragie catastrophique en phase préhospitalière est particulièrement complexe. Ces dernières années la mise en place d'un réseau structuré de prise en charge, 'application de procédures spécifiques visant à arrêter les hémorragies au plus tôt, le recours à l'acide tranexaminique, la prévention des hypothermies et l'application d'une politique raisonnée de rénaimation/chirurgie ont constitué une grande avancée. Certaines nations ont équipé leurs vecteurs d'évacuations de concentrés érythrocytaires. Le maintien d'une coagulation optimale est un enjeu majeur. Pour cela existe, entre autres, le plasma lyophilisé. Les forces armées israéliennes militent pour l'emploi de ce type de solutions en phase préhospitalière
| Tags : coagulopathie, hémorragie
29/06/2013
Coagulopathie du trauma: Que faire ?
Case Scenario: Management of Trauma-induced Coagulopathy in a Severe Blunt Trauma Patient
David JS et All. Anesthesiology 2013; 119:191–200
Un point très clair du problème
| Tags : coagulopathie
26/05/2013
Plasma lyophilisé: Une réalité
Le Service de Santé des Armées a recours depuis de nombreuses années (1, 2) à une présentation originale de plasma thérapeutique le PLYO.
Initialement réservé à un emploi en opérations extérieures, il vient d'être validé sous contraintes pour un usage sur le territoire national: Le plasma lyophilisé (PLYO) est principalement distribué aux unités médico-chirurgicales militaires déployées en Opérations Extérieures (OPEX) pour répondre aux contraintes logistiques du contexte opérationnel et à la nécessité de disposer, sans délai, de plasma pour le traitement des blessés hémorragiques. En milieu civil, le PLYO pourrait être utilisé par les établissements de santé présentant des difficultés logistiques majeures ne permettant pas d’assurer une chaîne du froid négative ou au cours de situations d’extrême urgence avec nécessité d’un apport de plasma thérapeutique sans délai. Dans cette deuxième indication, le PLYO devrait être utilisé en attendant que le plasma frais congelé soit décongelé et disponible. Le plasma lyophilisé français (PLyo®) préparé préférentiellement à partir de plasma frais congelé traité par l’amotosalen. Il est obtenu par lyophilisation à partir d’un mélange de PFC-IA issus d’aphérèse, provenant de dix donneurs différents au maximum, de groupes sanguins A, B, et AB, exempts d’anticorps immuns anti-A ou anti-B, conservés à une température inférieure ou égale à −25 °C.
Il en existe d'autres. Le plasma lyophilisé sud-africain (Bioplasma®) est le seul équivalent au monde du plasma lyophilisé français du fait de son universalité. Il s’agit d’un produit sud-africain bénéficiant d’une autorisation nationale depuis 1994 et commercialisé depuis 1996. Ce plasma est lyophilisé, universel et traité par solvant-détergent. Il existe en deux formats de flacon : 50 ou 200 mL. Le plasma lyophilisé allemand (LyoPlas N-W®), produit par le service de transfusion sanguine de la croix rouge allemande, provient d’un seul donneur de sang total ou d’aphérèse. Il n’est donc pas universel au regard de la compatibilité ABO. Le produit est sécurisé par quarantaine de quatre mois. Il peut être stocké 15 mois entre +2 et +25 °C.
Une révue récente fait le point sur les divers plasma thérapeutiques disponibles.
| Tags : coagulopathie
21/02/2013
Pour la coagulation: HEA de haut PM pas bon ?
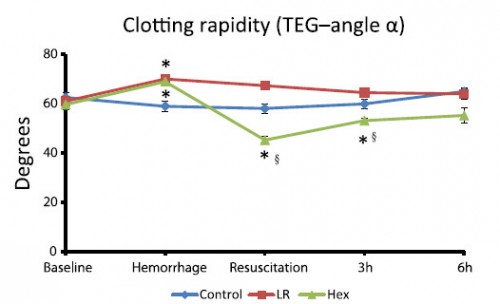
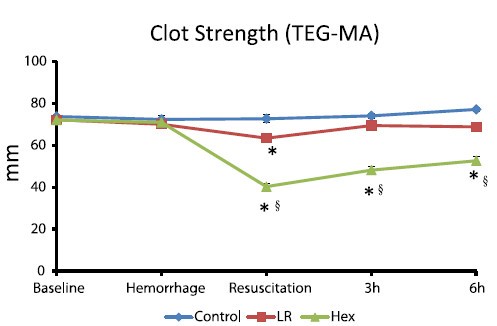
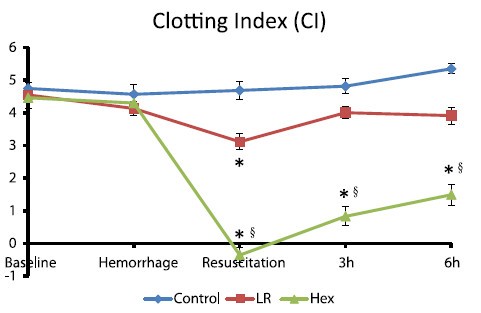
Comparisons of lactated Ringer’s and Hextend resuscitation on hemodynamics and coagulation following femur injury and severe hemorrhage in pigs
Wenjun Z et all J Trauma Acute Care Surg. 2013;74: 732-740
After traumatic hemorrhage, coagulation function was restored within 6 hours with LR resuscitation but not with Hextend. The lack of recovery after Hextend is likely caused by greater hemodilution and possible effects of starches on coagulation substrates and further documents the need to restrict the use of high-molecular-weight starch in resuscitation fluids for bleeding casualties.
On rappelle que l'Hextend est un HEA 670/0.75 et que le voluven est un HEA 130/0,4 dont les effets sur la coagulation sont réputées étant moindres.
| Tags : coagulopathie, remplissage, hémorragie
01/12/2012
Apport du fibrinogène: A la folie ou pas du tout ??
Une econférence qui fait parfaitement le point sur l'intérêt et les questions en suspens concernant l'intérêt du fibrinogène dans la réanimation hémostatique du traumasié qui saigne.
En condition de combat avant l'arivée en structure hopsitalière de campagne, l'apport de fibrinogène peut être réalisé par l'apport de plasma lyophylisé (PLYO) produit par le SSA (obtenu en moins de 6 min après reconstitution à température ambiante par adjonction d'eau PPI, chaque unité contient au moins 0,5g de fibrinogène). C'est une des composantes de la transfusion de plasma thérapeutique. qui doit désormais être envisagé au niveau du role 1 (poste de secours ou vecteur d'évacuation tactique).
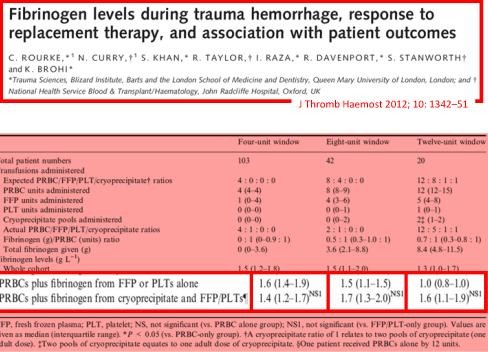
Le recours au fibrinogène (Clottafact), qui apparaît être d'un intérêt majeur compte tenu d'un apport insuffisant par la transfusion de plasma. (Abstract Rourke et all.)
Il ne peut (pour des raisons de logistique de production et de disponibilté) être apporté qu'à partir de la prise en charge hospitalière.
Pour approfondir avec en perspective le blessé de guerre hémorragique:
(1) Un revue générale sur la coagulopathie de l'hémorragie massive: "Hemodilution caused by trauma and major surgery induces complex hemostatic changes involving procoagulant factors as well as anticoagulant, fibrinolytic, and antifibrinolytic factors. The endothelial responses to shear stress, active proteases, and various inflammatory cells and cytokines add further complexity to the pathophysiology of massive hemodilution. In addition to the conventional transfusion products, which are often difficult to administer in a timely manner, purified factor concentrates of plasma origin and from recombinant synthesis are highly concentrated (i.e., small volume) for a rapid restoration of targeted factor(s). The use of point-of-care testing is desirable to optimize the dose and timing of such intervention. Additional clinical trials of different factor concentrate therapies are required to validate their efficacy and safety in patients after trauma or major surgery.152 Further understanding of the time course of pathophysiological changes in massive hemodilution is necessary to optimally balance hemostatic and anticoagulant therapies."
(2) Un focus sur le blessé de guerre: "In patients with combatrelated trauma requiring massive transfusion, the transfusion of an increased fibrinogen: RBC ratio was independently associated with improved survival to hospital discharge, primarily by decreasing death from hemorrhage. Prospective studies are needed to evaluate the best source of fibrinogen and the optimal empiric ratio of fibrinogen to RBCs in patients requiring massive transfusion."
(3) La stratégie transfusionnelle du blessé de guerre SFAR 2012: " En traumatologie, l’administration de fibrinogène est recommandée : dose initiale de 3 à 4 g suivie d’une administration régulière en cas d’hypofibrinogènémie biologique (<1,5 à 2 g/l) ou de signes thromboelastométriques de déficit fonctionnel en fibrinogène [8]. Une analyse nord-américaine rétrospective de 252 dossiers de BdG ayant nécessité une TM a permis de mettre en évidence qu’un apport faible de fibrinogène (< 0,2 g/CGR) au cours de la transfusion était associé à une majoration significative de la mortalité de ces blessés [39]. Le SSA américain utilise l’apport de cryoprécipités contenant surtout du fibrinogène et d’autres facteurs de coagulation pour compenser ces déficits [37]. Les recommandations du SSA français sont l’administration de fibrinogène de façon répétée afin de maintenir un fibrinogène plasmatique supérieur à 1,5 g/l ou en l’absence de laboratoire (situation des structures chirurgicales « légères »), d’administrer au moins 0,2 g de fibrinogène par CGR transfusé."
| Tags : coagulopathie
23/09/2012
Facteur VIIa: Intérêt pas prouvé !
Use of recombinant factor VIIA for control of combat-related haemorrhage.
Woodruff SI et all. Emerg Med J 2010;27:2 121-124
Ce travail met en exergue que le recours au FVIIa n'a pas d'intérêt prouvé en cas de prise en charge de traumatismes pénétrants. Ceci est d'autant plus vrai qu'il est fait alors qu'une coagulopathie sévère est installée (The utility of recombinant factor VIIa as a last resort in trauma. Mamtani R. et all. World Journal of Emergency Surgery 2012, 7(Suppl 1):S7)
----------------------------------------------
Background
Recombinant activated human coagulation factor VII (rFVIIa), an intravascular strategy to promote clotting, is being used as an adjunct to surgical control of bleeding in combat trauma patients.
Objective
To describe the initial experiences with rFVIIa administered to combat casualties at US Navy-Marine Corps medical treatment facilities in Iraq, and to comparesurvival outcomes of those treated with rFVIIa to controls not receiving rFVIIa.
Methods
Medical encounter data from the US Navy-Marine Corps Combat Trauma Registry were retrospectively reviewed to identify all battle-injured patients documented as having received rFVIIa during the period May 2004 to January 2006 of Operation Iraqi Freedom. Available clinical and injury related data are presented to characterise the patients. To assess effects of rFVIIa on survival outcomes, rFVIIa cases were matched to controls on injury severity and age.
Results
22 battle-injured patients from the Combat Trauma Registry received rFVIIa. Primarily young US Marines, these patients typically had penetrating injuries from improvised explosive devices and gunshot wounds. Injuries were often abdominal. The average dose used was similar to that reported in another study of civilian trauma patients, although dosing varies widely in the existing experimental and anecdotal literature. Over two-thirds (68%) of the rFVIIa patients surviveddan identical outcome seen for a matched control group of 22 patients.
Conclusions
Survival of seriously injured combat casualties was good, although identical to that of a control group. Methodological limitations of this retrospective study preclude making firm conclusions about the effectiveness of rFVIIa. Future controlled studies are needed for safety and efficacy testing of rFVIIa in combat trauma patients.
----------------------------------------------
| Tags : hémorragie, coagulopathie